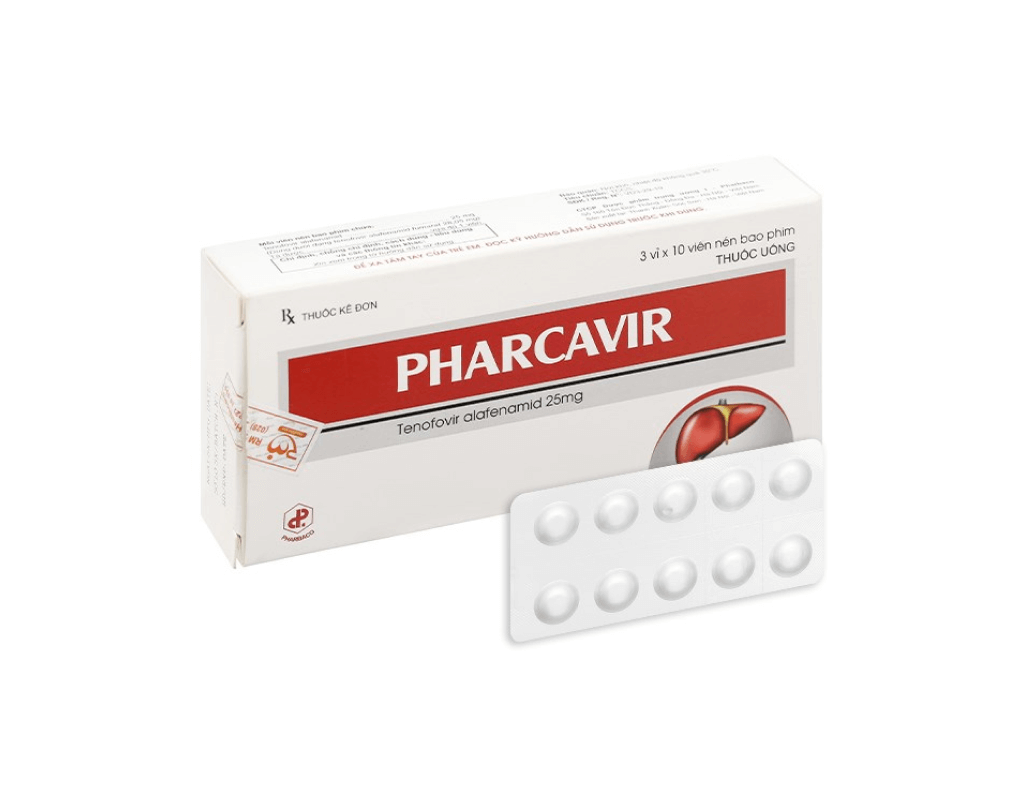
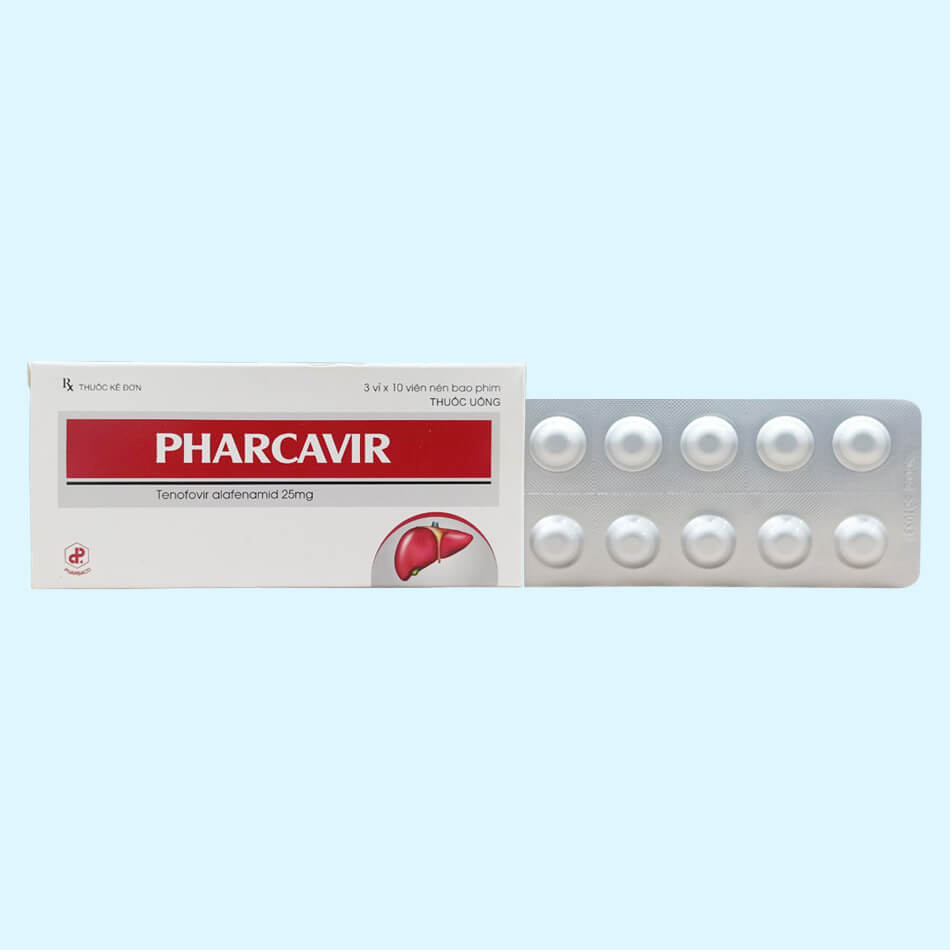
Pharcavir 25mg
Giá:
Công dụng: Điều trị bệnh viêm gan siêu vi B mạn tính.
Thành phần chính: Tenofovir
Đối tượng sử dụng: Từ 12 tuổi trở lên với cân nặng ≥ 35kg
Thương hiệu: Dược phẩm Trung Ương 1 – Pharbaco (Việt Nam)
Hãng sản xuất: Pharbaco
Nơi sản xuất: Việt Nam
Dạng bào chế: Viên nén bao phim
Cách đóng gói: 3 vỉ x 10 viên
Thuốc cần kê toa: Có
Hạn dùng: 36 tháng kể từ ngày sản xuất.
Số đăng kí: VD3-29-19
THÔNG TIN SẢN PHẨM
Thành phần của Thuốc Pharcavir 25mg
Thông tin thành phần: Tenofovir alafenamide
Hàm lượng: 25mg
Công dụng của Thuốc Pharcavir 25mg
Chỉ định
Thuốc Phacavir 25mg được chỉ định dùng trong các trường hợp sau:
Chỉ định điều trị viêm gan B mạn tính ở người lớn và thanh thiếu niên (từ 12 tuổi trở lên với cân nặng ≥ 35 kg).
Dược lực học
Tenofovir alafenamide fumarate (viết tắt TAF), TAF là tiền chất phosphoramidite của Tenofovir. Sau khi vào trong cơ thể nó được vận chuyển hoặc khuếch tán thụ động vào các tế bào gan. TAF sau đó được thủy phân thành Tenofovir, rồi được phosphoryl hóa thành dạng có hoạt tính là Tenofovir diphosphat.
Tenofovir diphosphat ức chế sự sao chép của HBV (vi rút viêm gan B) thông qua ức chế men sao chép ngược HBV polymerase dẫn đến kết thúc chuỗi DNA của vi rút.
Dược động học
Sau khi uống tenofovir alafenamide trong điều kiện nhịn ăn ở bệnh nhân người lớn bị viêm gan B mãn tính, nồng độ đỉnh trong huyết tương của tenofovir alafenamide được quan sát thấy sau khoảng 0,48 giờ. So sánh với khi nhịn đói, việc dùng một liều tenofovir alafenamide duy nhất với bữa ăn nhiều chất béo làm tăng 65% lượng tenofovir alafenamide tiếp xúc với cơ thể.
Sự gắn kết của tenofovir alafenamide với protein huyết tương của người trong các mẫu thu thập trong các nghiên cứu lâm sàng là khoảng 80%. Liên kết của tenofovir với protein huyết tương của người là dưới 0,7%.
Chuyển hóa là con đường thải trừ chủ yếu của tenofovir alafenamide ở người, chiếm > 80% liều uống. Các nghiên cứu in vitro cho thấy tenofovir alafenamide được chuyển hóa thành tenofovir (chất chuyển hóa chính) bởi carboxylesterase-1 trong tế bào gan; và bằng cathepsin A trong tế bào đơn nhân máu ngoại vi (PBMC) và đại thực bào.
Bài tiết tenofovir alafenamide nguyên vẹn qua thận không đáng kể với <1% liều dùng được thải trừ qua nước tiểu. Tenofovir alafenamide được thải trừ chủ yếu sau khi chuyển hóa thành tenofovir. Tenofovir được thải trừ khỏi cơ thể qua thận bằng cả quá trình lọc ở cầu thận và bài tiết tích cực ở ống thận.
Cách dùng Thuốc Pharcavir 25mg
Cách dùng
Thuốc Phacavir 25mg dùng đường uống, nên dùng thuốc cùng với thức ăn.
Nên uống thuốc cùng vào một thời điểm trong ngày.
Nếu bệnh nhân bị nôn trong vòng một giờ sau khi uống thuốc, bệnh nhân cần dùng 1 viên thuốc khác. Nếu bệnh nhân bị nôn mửa hơn 1 giờ sau khi uống thuốc, không cần dùng thêm viên thuốc khác.
Liều dùng
Người lớn và thanh thiếu niên (từ 12 tuổi trở lên với cân nặng ≥ 35 kg): 1 viên/lần x 1 lần/ngày.
Ở những bệnh nhân HBeAg dương tính, không xơ gan: Điều trị nên được tiến hành ít nhất 6-12 tháng sau khi xác định có huyết thanh chuyển đổi HBe (HBeAg âm tính, không phát hiện được ADN của virus viêm gan B và có kháng thể HBe) hoặc tới khi có huyết thanh chuyển đổi HBs hoặc khi thấy thuốc mất tác dụng. Khuyến cáo đánh giá lại thường xuyên sau khi ngừng điều trị để phát hiện sự tái phát virus.
Ở những bệnh nhân HBeAg âm tính, không xơ gan: Điều trị phải kéo dài cho đến khi huyết thanh chuyển đổi HBs hoặc cho đến khi thấy thuốc không còn tác dụng. Với điều trị kéo dài hơn 2 năm, nên đánh giá lại thường xuyên để chắc chắn rằng việc tiếp tục lựa chọn liệu pháp vẫn còn thích hợp cho bệnh nhân.
Người cao tuổi: Không cần điều chỉnh liều ở bệnh nhân từ 65 tuổi trở lên.
Bệnh nhân suy thận: Không cần điều chỉnh liều ở những bệnh nhân người lớn và thanh thiếu niên (từ 12 tuổi trở lên với cân nặng ≥ 35 kg) và có độ thanh thải creatinin ≥ 15 ml/phút hoặc ở những bệnh nhân thẩm tách máu và có độ thanh thải creatinin < 15 ml/phút. Không có mức liều khuyến cáo cho bệnh nhân có độ thanh thải creatinin < 15 ml/phút và không thẩm tách máu.
Suy gan: Không cần điều chỉnh liều Pharcavir ở bệnh nhân suy gan.
Trẻ em: Tính an toàn và hiệu quả của Pharcavir ở trẻ em dưới 12 tuổi hoặc nặng < 35 kg chưa được xác lập, các dữ liệu chưa có sẵn.
Lưu ý: Liều dùng trên chỉ mang tính chất tham khảo. Liều dùng cụ thể tùy thuộc vào thể trạng và mức độ diễn tiến của bệnh. Để có liều dùng phù hợp, bạn cần tham khảo ý kiến bác sĩ hoặc chuyên viên y tế.
Làm gì khi dùng quá liều?
Điều trị quá liều tenofovir alafenamide bao gồm các biện pháp hỗ trợ chung bao gồm theo dõi các dấu hiệu sinh tồn cũng như theo dõi tình trạng lâm sàng của bệnh nhân.
Tenofovir được loại bỏ hiệu quả bằng lọc thận với hệ số chiết xuất xấp xỉ 54%. Người ta không biết liệu tenofovir có thể được loại bỏ bằng thẩm phân phúc mạc hay không.
Làm gì khi quên 1 liều?
Bổ sung liều ngay khi nhớ ra. Tuy nhiên, nếu thời gian giãn cách với liều tiếp theo quá ngắn thì bỏ qua liều đã quên và tiếp tục lịch dùng thuốc. Không dùng liều gấp đôi để bù cho liều đã bị bỏ lỡ.
Nếu bệnh nhân quên một liều uống ngay khi nhớ ra (nếu thời gian chưa quá 18 giờ) và uống liều tiếp theo như bình thường. Nếu thời gian vượt quá 18 giờ thì không uống liều đã quên và uống liều tiếp theo như bình thường.
Tác dụng phụ
Khi sử dụng thuốc Phacavir 25mg, bạn có thể gặp các tác dụng không mong muốn (ADR).
Thường gặp, ADR >1/100
Thần kinh: Đau đầu, chóng mặt.
Tiêu hoá: Tiêu chảy, nôn, buồn nôn, đau bụng, chướng bụng, đầy hơi.
Gan mật: Tăng ALT.
Da và mô dưới da: Ngứa, phát ban.
Cơ xương khớp: Đau cơ.
Toàn thân: Mệt mỏi.
Ít gặp, 1<1000: ADR < 1/100
Da và mô dưới da: Phù mạch, mề đay.
Hướng dẫn cách xử trí ADR
Khi gặp tác dụng phụ của thuốc, cần ngưng sử dụng và thông báo cho bác sĩ hoặc đến cơ sở y tế gần nhất để được xử trí kịp thời.
Lưu ý
Trước khi sử dụng thuốc bạn cần đọc kỹ hướng dẫn sử dụng và tham khảo thông tin bên dưới.
Chống chỉ định
Thuốc Phacavir 25mg chống chỉ định trong các trường hợp sau:
Quá mẫn cảm với tenofovir alafenamid fumarat hoặc bất cứ các thành phần nào của thuốc.
Thận trọng khi sử dụng
Truyền nhiễm HBV
Bệnh nhân phải được thông báo rằng viên nén tenofovir alafenamide không ngăn ngừa được nguy cơ lây truyền HBV sang người khác thông qua quan hệ tình dục hoặc đường máu. Phải tiếp tục sử dụng các biện pháp phòng ngừa thích hợp.
Các bệnh nhân bị bệnh gan mất bù
Không có dữ liệu an toàn và hiệu quả của viên nén tenofovir alafenamide ở những bệnh nhân nhiễm HBV có bệnh gan mất bù và có điểm số Child Pugh Turcotte (CPTP9 (nghĩa là cấp C). Những bệnh nhân này có nguy cơ cao bị tác dụng không mong muốn nghiêm trọng lên gan và thận. Vì vậy, các thông số về gan mật và thận nên được theo dõi chặt chẽ trong nhóm bệnh nhân này.
Sự trầm trọng hơn của viêm gan
Bùng phát trong điều trị:
Sự gia tăng tự phát trong viêm gan B mạn tính là tương đối phổ biến và được đặc trưng bởi sự gia tăng thoáng qua alanine aminotransferase (ALT) trong huyết thanh. Sau khi bắt đầu điều trị bằng thuốc kháng virus, ALT huyết thanh có thể tăng trong một vài bệnh nhân.
Trong các bệnh nhân có bệnh gan còn bù, sự gia tăng ALT huyết thanh nói chung không đi kèm với tăng nồng độ bilirubin huyết thanh hoặc sự mất bù gan. Các bệnh nhân xơ gan có nguy cơ cao hơn sự mất bù gan sau khi viêm gan trầm trọng hơn, và vì vậy nên được theo dõi chặt chẽ trong quá trình điều trị.
Bùng phát sau khi ngừng điều trị:
Đợt kịch phát cấp của viêm gan đã được báo cáo ở các bệnh nhân đã ngừng điều trị viêm gan B, thường liên quan đến sự tăng nồng độ HBV DNA trong huyết tương. Phần lớn các trường hợp là tự giới hạn bản thân nhưng kịch phát nghiêm trọng, bao gồm cả tử vong, có thể xảy ra sau khi ngừng điều trị viêm gan B.
Chức năng gan phải được theo dõi trong khoảng thời gian lặp lại với cả lâm sàng và xét nghiệm trong ít nhất 6 tháng sau khi ngưng điều trị viêm gan B. Nếu thích hợp, việc tiếp tục điều trị viêm gan B có thể được bảo đảm.
Trong các bệnh nhân bị bệnh gan tiến triển hoặc xơ gan, ngưng điều trị không được khuyến cáo vì sau đợt điều trị kịch phát của viêm gan có thể dẫn đến sự mất bù của gan. Sự bùng phát của gan đặc biệt nghiêm trọng, và đôi khi gây tử vong ở bệnh nhân bị bệnh gan mất bù.
Suy thận
Bệnh nhân với độ thanh thải creatinine < 30 mL/phút.
Việc sử dụng viên nén tenofovir alafenamide mỗi lần một ngày ở bệnh nhân có CrCl2 15 mL/phút nhưng < 30 mL/phút và bệnh nhân có CrCl<15 mL/phút đang chạy thận nhân tạo được dựa trên dữ liệu được động học giới hạn và trên mô hình hóa và mô phỏng. Không có dữ liệu an toàn trên việc sử dụng viên nén tenofovir alafenamide để điều trị nhiễm HBV ở bệnh nhân có CrCl< 30 mL/phút.
Sử dụng viên nén tenofovir alafenamide không được khuyến cáo ở bệnh nhân có CrCl< 15 mL/phút mà không chạy thận nhân tạo.
Độc thân
Nguy cơ tiềm ẩn của độc thân do phơi nhiễm mãn tính ở mức thấp tenofovir do dùng tenofovir alafenamide không thể bị loại trừ.
Bệnh nhân nhiễm đồng thời HBV và viêm gan virus C hoặc D
Không có dữ liệu an toàn và hiệu quả của viên nén tenofovir alafenamide trong bệnh nhân nhiễm đồng thời với viêm gan virus C hoặc D. Nên theo dõi hướng dẫn sử dụng kết hợp cho điều trị viêm.
Viêm gan B và nhiễm đồng thời HIV
Kiểm tra kháng thể HIV nên được đề nghị cho tất cả các bệnh nhân nhiễm HBV ở những người tình trạng nhiễm HIV-1 chưa được biết trước khi bắt đầu điều trị với viên nén tenofovir alafenamide. Trong những bệnh nhân bị nhiễm đồng thời HBV và HIV, viên nén tenofovir alafenamide nên được sử dụng đồng thời với các tác nhân khác kháng tetrovirus để đảm bảo rằng bệnh nhân nhận được phác đồ thích hợp cho điều trị HIV.
Khả năng lái xe và vận hành máy móc
Không có hoặc ảnh hưởng không đáng kể đến khả năng lái xe và sử dụng máy móc. Bệnh nhân nên được thông báo rằng chóng mặt đã được báo cáo trong khi điều trị với tenofovir alafenamide.
Thời kỳ mang thai
Không có hoặc có số lượng dữ liệu hạn chế (ít hơn 300 kết quả) về việc sử dụng tenofovir alafenamide ở phụ nữ mang thai. Tuy nhiên, một lượng lớn dữ liệu về phụ nữ mang thai (hơn 1.000 kết cục bị phơi nhiễm) cho thấy không có dị tật cũng như độc tính đối với thai nhi/trẻ sơ sinh liên quan đến việc sử dụng tenofovir disoproxil.
Các nghiên cứu trên động vật không chỉ ra tác hại trực tiếp hoặc gián tiếp đối với độc tính sinh sản
Việc sử dụng tenofovir alafenamide có thể được xem xét trong thời kỳ mang thai, nếu cần thiết.
Thời kỳ cho con bú
Người ta không biết liệu tenofovir alafenamide có được tiết vào sữa mẹ hay không. Tuy nhiên, trong các nghiên cứu trên động vật, người ta đã chỉ ra rằng tenofovir được tiết vào sữa. Không có đủ thông tin về tác dụng của tenofovir ở trẻ sơ sinh/trẻ nhỏ.
Không thể loại trừ rủi ro đối với trẻ sơ sinh/trẻ sơ sinh bú sữa mẹ; do đó, không nên dùng tenofovir alafenamide trong thời kỳ cho con bú.
Tương tác thuốc
Acyclovir – Valacyclovir, Adefovir, Aminoglycoside, Cabozantinib, Cidofovir, Ganciclovir – Valganciclovir… Pharcavir có thể làm tăng nồng độ các thuốc này trong huyết tương.
Carbamazepine, Fosphenytoin – phenytoin, Orlistat, Oxcarbazepine phenobarbital, Primidone, Rifabutin, Rifampin, Rifapentine, Tipranavir,… làm giảm nồng độ Tenofovir alafenamide trong huyết tương.
Cladribine: Tenofovir alafenamide làm giảm tác dụng điều trị của thuốc Cladribine.
Chống viêm không steroid (NSAIDs): Tăng cường tác dụng thải độc thận của Tenofovir alafenamide.
Bảo quản
Bảo quản không quá 30 °C.